Summary
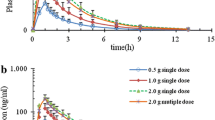
After intravenous injection of single doses of 1.0 g of cefpirome (HR 810) and multiple doses of 1.0 g b.i.d. for five days to the same ten healthy male volunteers in an open design, concentrations of unchanged drug were estimated at various times in serum and urine, over 24 h and 48 h, respectively. Cefpirome concentrations were determined using both high pressure liquid chromatography (HPLC) and a microbiological assay. The measurements obtained were compared by linear distribution independent regression, and were found to be equivalent, indicating no major antimicrobially active metabolites of cefpirome. Biological half-life (t1/2,β) was determined by fitting a two-compartment open model to the data: t1/2,β was 2 h (HPLC, median values). During the multiple dose phase of cefpirome (1.0 g b.i.d.) no accumulation of the serum levels could be detected with this dosage regimen. Urinary concentrations of unchanged cefpirome remained clearly above the minimal inhibitory concentration forEscherichia coli (0.03 mg/l) for about 36 h (microbiological assay). The general tolerance was good.
Zusammenfassung
Die Serum- und Harnwirkstoff-Konzentrationen von unverändertem Cefpirom (HR 810) wurden in einer offenen Studie bei denselben zehn Probanden über 24 bzw. 48 Studen nach einer intravenösen Injektion von 1,0 g Cefpirom täglich und von 1,0 g Cefpirom zweimal täglich für fünf Tage untersucht. Cefpirom-Konzentrationen wurden mit Hilfe von Hochdruckflüssigkeitschromatographie (HPLC) und auch einer mikrobiologischen Methode bestimmt. Die Ergebnisse wurden mit einer linearen verteilungsunabhängigen Regression verglichen und für gleichwertig befunden, was darauf schließen läßt, daß keine wesentlichen Anteile von antimikrobiell aktiven Metaboliten gebildet werden. Die biologische Halbwertszeit (t1/2,β), bestimmt mit Hilfe eines offenen Zwei-Kompartimenten-Modells, betrug ca. zwei Stunden (HPLC, mediane Werte). Während der Mehrfachapplikation von 1,0 g Cefpirom zweimal täglich konnten keine Akkumulationen der Serumwerte mit diesem Dosisschema festgestellt werden. Die Wirkstoff-Konzentrationen von unverändertem Cefpirom im Harn blieben für etwa 36 Stunden (Mikrobiologische Methode) deutlich über der minimalen Hemmkonzentration fürEscherichia coli (0,03 mg/l). Die allgemeine Verträglichkeit war gut.
Similar content being viewed by others
Literature
Seibert, G., Klesel, N., Limbert, M., Schrinner, E., Seeger, K., Winkler, I., Lattrell, R., Blumbach, J., Dürckheimer, W., Fleischmann, K., Kirrstetter, R., Mencke, B., Ross, B. C., Scheunemann, K.-H., Schwab, W., Wieduwilt, M. HR 810, a new parenteral cephalosporin with a broad antibacterial spectrum. Arzneim.-Forsch./Drug Res. 33 (1983) 1084–1086.
Seibert, G., Limbert, M., Winkler, I., Dick, T. The antibacterial activityin vitro and β-lactamase stability of the new cephalosporin HR 810 in comparison with five other cephalosporins and two aminoglycosides. Infection 11 (1983) 275–279.
Passing, H., Bablok, W. A new biometrical procedure for testing the equality of measurements from two different analytical methods. J. Clin. Chem. Biochem. 21 (1983) 709–720.
Wagner, J. G. Fundamentals of clinical pharmacokinetics, 2nd ed. Drug Intelligence publications, Hamilton, Illinois, 1979.
Elfring, G. L., Metzler, C. M. The efficient use of NONLIN for unbalanced multiple dose data. J. Pharmacok. Biopharmaceutics 9 (1981) 497–501.
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Maaß, L., Verho, M., Rangoonwala, R. et al. Single and multiple dose pharmacokinetics of intravenous cefpirome (HR 810), a novel cephalosporin derivative. Infection 15, 211–214 (1987). https://doi.org/10.1007/BF01646053
Issue Date:
DOI: https://doi.org/10.1007/BF01646053