Summary
The fine structure of the smooth fibers from the anterior byssus retractor muscle (ABRM) of the mussel Mytilus edulis was investigated in the relaxed and in the contracted state.
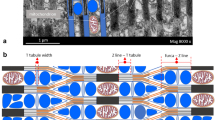
Most of the fiber volume is occupied by the contractile apparatus. There are thick (between 170 and 800 Å) and thin (about 60 Å diameter) myofilaments. The last ones are attached to spindle shaped Z-elements which lie among the myofilaments at irregular intervals and sometimes appear to be connected with the plasma-membrane.
The myofilaments run parallel to each other, but no other regularity is apparent from longitudinal sections. Cross-sections, however, show the presence of irregular “A zones” and “I zones” in these smooth muscle fibers. Contraction leads to a considerable increase in the number of myofilaments per cross-sectional area. This indicates that shortening takes place according to the sliding filament theory.
Relaxed fibers seem to be uniform, while contracted ones may differ in their appearence. In those three distinct patterns were observed in the distribution of myofilaments:
-
1.
Thick and thin myofilaments are distributed rather evenly across the whole cross-sectional area.
-
2.
The thick myofilaments are arranged in irregular groups. In each group the filaments touch each other especially in their middle portions. Therefore, it is sometimes difficult to recognize the outline of a particular single filament. Most of the thin filaments occupy the space between the groups of thick filaments.
-
3.
The thick myofilaments are crowded in a central area of the fiber. Here they aggregate, so that little or no interval is left between individual filaments. Most of the thin filaments are found in a peripheral zone of the fiber.
These observations are discussed in view of possible correlations to the different functional states of the ABRM: phasic and tonic contraction.
Zusammenfassung
Die glatten Fasern aus dem vorderen Byssusretraktor (ABRM) der Miesmuschel Mytilus edulis wurden elektronenmikroskopisch untersucht. Unsere besondere Aufmerksamkeit richtete sich dabei auf die Veränderungen, die beim Übergang des erschlafften Zustands in den kontrahierten eintreten.
Der kontraktile Apparat, der fast das gesamte Faservolumen einnimmt, besteht aus dicken (170–800 Å) und dünnen (etwa 60 Å) Myofilamenten sowie aus länglichen Z-Elementen, an deren Schmalseiten die dünnen Myofilamente ansetzen. Auf Längsschnitten ist außer einer Parallelorientierung der Myofilamente keinerlei Regelmäßigkeit zu erkennen. Querschnitte zeigen das Vorhandensein von undeutlich umrissenen „A-Zonen“ und „I-Zonen“.
Die Kontraktion ist mit einer erheblichen Vermehrung der Myofilamente im Faserquerschnitt und der Dichte ihrer Packung verbunden. Dies kann als ein Anzeichen für eine Verkürzung durch einen Gleitmechanismus angesehen werden.
Im Gegensatz zu den erschlafften Fasern sind die kontrahierten uneinheitlich strukturiert. Im Hinblick auf Anordnung und Verteilung der beiden Myofilamenttypen wurden drei verschiedene Muster beobachtet:
-
1.
Dicke und dünne Myofilamente liegen ziemlich gleichmäßig über den ganzen Querschnitt verteilt.
-
2.
Die dicken Myofilamente bilden unregelmäßige und unvollständig voneinander abgegrenzte Gruppen, innerhalb derer die Einzelfilamente vor allem mit ihren Mittelteilen so eng aneinandergelagert sind, daß sich ihr Umriß häufig nur schwierig erkennen läßt. Die Masse der dünnen Filamente liegt in den Zwischenräumen zwischen den Gruppen der dicken.
-
3.
Die dicken Myofilamente finden sich nur in einer zentralen Zone der Faser. Sie liegen hier ebenfalls eng aneinandergepreßt („aggregiert“). Die meisten dünnen Myofilamente sind in eine periphere Zone verlagert.
Diese Befunde werden im Hinblick auf mögliche Korrelationen mit den verschiedenen Funktionszuständen des ABRM, also der phasischen Kontraktion und dem Sperrtonus diskutiert.
Similar content being viewed by others
Literatur
Bouligand, Y.: La disposition des myofilaments chez une annélide polychète. J. Microscopie 5, 305–322 (1966).
Brandt, P. W., J. P. Reuben, L. Giradier, and H. Grundfest: Correlated morphological and physiological studies on isolated single muscle fibers. J. Cell Biol. 25, 233–260 (1965).
Caesar, R., G. E. Edwards, and H. Ruska: Architecture and nerve supply of mammalian smooth muscle tissue. J. biophys. biochem. Cytol. 3, 867–877 (1957).
Elliott, G. F.: Electron microscope studies of the structure of the filaments in the opaque adductor muscle of the oyster Crassostrea angulata. J. molec. Biol. 10, 89–104 (1964).
Fawcett, D. W., and C. C. Selby: Observations on the fine structure of the turtle atrium. J. biophys. biochem. Cytol. 4, 63–71 (1958).
Fletcher, C. M.: Action potentials recorded from an unstriated muscle of simple structure. J. Physiol. (Lond.) 90, 233–253 (1937).
Hanson, J., and J. Lowy: Evidence for a sliding filament contractile mechanism in tonic smooth muscles of lamellibranch molluscs. Nature (Lond.) 184, 286–287 (1959).
—: The structure of musle fibres in the translucent part fo the adductor of the oyster Crassostrea angulata. Proc. roy. Soc. B 154, 173–196 (1961).
—: The structure of F-actin filaments isolated from muscle. J. molec. Biol. 6, 46–60 (1963).
—: The structure of molluscan tonic muscles. In: Biochemistry of muscle contraction (J. Gergely, ed.), p. 400–411. London: J.& A. Churchill Ltd. 1964.
—, H. E. Huxley, K. Bailey, C. M. Kay, and J. C. Rüegg: Structure of molluscan tropomyosin. Nature (Lond.) 180, 1134–1135 (1957).
Heumann, H.-G.: Diss. Heidelberg 1967.
—, u. E. Zebe: Über Feinbau und Funktionsweise der Fasern aus dem Hautmuskelschlauch des Regenwurms, Lumbricus terrestris L. Z. Zellforsch. 78, 131–150 (1967).
Huxley, H. E.: The double array of filaments in cross striated muscle. J. biophys. biochem. Cytol. 3, 631–648 (1957).
Ikemoto, N.: Further studies in electron microscopic structures of the oblique-striated muscle of the earthworm Eisenia foetida. Biol. J. Okayama Univ. 9, 81–126 (1963).
Johnson, W. H.: Fibrous protein systems in muscle. In: Ultrastructure of protein fibers (R. Borasky ed.), p. 139–176. New York and London: Academic Press 1963.
Locker, H. A., and F. O. Schmitt: Some chemical and structural properties of paramyosin. J. biochem. biophys. Cytol. 3, 889–896 (1957).
Lowy, J., and J. Hanson: Ultrastructure of invertebrate smooth muscles. Physiol. Rev. 42 (Suppl. 5), 34–47 (1962).
—, and B. M. Millman: The contractile mechanism of the anterior byssus retractor muscle of Mytilus edulis. Phil. Trans. B 246, 105–148 (1963).
MacRae, E. K.: Observations on the fine structure of the pharyngeal muscle in the planarian Dugesia tigrina. J. Cell Biol. 18, 651–662 (1963).
—: The fine structure of muscle in a marine turbellarian. Z. Zellforsch. 68, 348–362 (1965).
Morita, M.: Electron microscopic studies on planaria. I. Fine structure of muscle fiber in the head of the planarian Dugesia dorotocephala. J. Ultrastruct. Res. 13, 383–395 (1965).
Nauss, K. M., and R. E. Davies: Changes in inorganic phosphate and arginine during the development, maintenance and loss of tension in the anterior byssus retractor muscle of Mytilus edulis. Biochem. Z. 345, 173–187 (1966).
Nieuwenhoven, S. J. van: An investigation into the structure and function of the anterior byssal retractor muscle of Mytilus edulis. Ph. D. thesis, Utrecht 1947.
Palade, G. E.: The fixation of tissues for electron microscopy. J. exp. Med. 95, 285–297 (1952).
Philpott, D. E., M. Kahlbrock, and A. G. Szent-Györgyi: Filamentous organization of molluscan muscles. J. Ultrastruct. Res. 3, 254–269 (1960).
Reynolds, E. S.: The use of lead citrate at high pH as an electron opaque stain in electron microscopy. J. Cell Biol. 17, 208–212 (1963).
Röhlich, P.: The fine structure of the muscle fiber of the leech Hirudo medicinalis. J. Ultrastruct. Res. 7, 399–408 (1962).
Rosenbluth, J.: Ultrastructural organization of obliquely striated muscle fibers in Ascaris lumbricoides. J. Cell Biol. 25, 495–515 (1965).
—: Obliquely striated muscle. III. Contraction mechanism of Ascaris body muscle. J. Cell Biol. 34, 15–33 (1967).
Rüegg, J. C.: A biochemical approach to the catch problem. In: Biochemistry of muscle contraction (J. Gergely ed.), p. 412–421. London: J. & A. Churchill Ltd. 1964.
—: Physiologie und Biochemie des Sperrtonus. Experimentelle Untersuchung mit besonderer Berücksichtigung des M. retractor byssi von Mytilus edulis. Helv. physiol. pharmacol. Acta, Suppl. 16, 1–76 (1965).
Sabatini, D. D., K. Bensch, and R. J. Barrnett: Cytochemistry and electron microscopy. The preservation of cellular ultrastructure and enzymatic activity by aldehyde fixation. J. Cell Biol. 17, 19–58 (1963).
Shoenberg, C. F.: Some electron microscope observations on the contraction mechanism in vertebrate smooth muscle. Proc. 5th Int. Congr. Electron Microscopy, Philadelphia 2, M-8 (1962).
—, J. C. Rüegg, D. M. Needham, R. H. Shirmer, and H. Nemetschek-Gansler: A biochemical and electron microcope study of the contractile proteins in vertebrate smooth muscle. Biochem. Z. 345, 255–266 (1966).
Stempak, J. G., and R. T. Ward: An improved staining method for electron microscopy. J. Cell Biol. 22, 697–701 (1964).
Twarog, B. M.: Responses of a molluscan smooth muscle to acetylcholine and 5-hydroxytryptamine. J. cell. comp. Physiol. 44, 141–163 (1954).
—: The regulation of catch in molluscan muscle. J. gen. Physiol. 50, 157–169 (1967).
Winton, F. R.: The changes in viscosity of an unstriated muscle (Mytilus edulis) during and after stimulation with alternating, interrupted and uninterrupted direct currents. J. Physiol. (Lond.) 88, 492–511 (1937).
Zebe, E., u. W. Rathmeyer: Unveröffentlichte Ergebnisse.
Author information
Authors and Affiliations
Additional information
Mit Unterstützung durch die Deutsche Forschungsgemeinschaft.
Rights and permissions
About this article
Cite this article
Heumann, H.G., Zebe, E. Über die Funktionsweise glatter Muskelfasern Elektronenmikroskopische Untersuchungen am Byssusretraktor (ABRM) von Mytilus edulis . Z. Zellforsch. 85, 534–551 (1968). https://doi.org/10.1007/BF00324747
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF00324747